2025年10月,安徽省药品监督管理局共批准首次注册第二类医疗器械产品18个,产品相关信息见附件。
特此公告。
附件:安徽省第二类医疗器械首次注册产品目录(2025年10月).xls
安徽省药品监督管理局
2025年11月13日
| 安徽省第二类医疗器械首次注册产品目录(2025年10月) | ||||
| 序号 | 产品名称 | 注册人名称 | 注册证号 | 批准日期 |
| 1 | 25-羟基维生素D检测试剂盒(液相色谱-串联质谱法) | 拜谱医疗科技(安徽)有限公司 | 皖械注准20252400237 | 2025年10月29日 |
| 2 | 一次性等离子手术电极 | 合肥臻创医疗科技有限公司 | 皖械注准20252010236 | 2025年10月29日 |
| 3 | 睡眠呼吸机 | 安徽双熙医疗设备有限公司 | 皖械注准20252080235 | 2025年10月29日 |
| 4 | 总三碘甲状腺原氨酸(TT3)检测试剂盒(化学发光法) | 必欧瀚生物技术(合肥)有限公司 | 皖械注准20252400234 | 2025年10月21日 |
| 5 | 总甲状腺素(TT4)检测试剂盒(化学发光法) | 必欧瀚生物技术(合肥)有限公司 | 皖械注准20252400233 | 2025年10月21日 |
| 6 | 游离三碘甲状腺原氨酸(FT3)检测试剂盒(化学发光法) | 必欧瀚生物技术(合肥)有限公司 | 皖械注准20252400232 | 2025年10月21日 |
| 7 | 促甲状腺激素检测试剂盒(化学发光法) | 必欧瀚生物技术(合肥)有限公司 | 皖械注准20252400231 | 2025年10月21日 |
| 8 | 游离甲状腺素(FT4)检测试剂盒(化学发光法) | 必欧瀚生物技术(合肥)有限公司 | 皖械注准20252400230 | 2025年10月20日 |
| 9 | 定制式矫治器 | 安庆宏峰医疗科技有限公司 | 皖械注准20252170229 | 2025年10月20日 |
| 10 | 维生素研究仪 | 安徽九陆生物科技有限公司 | 皖械注准20252220228 | 2025年10月20日 |
| 11 | 驾驶员体检机 | 安徽三联机器人科技有限公司 | 皖械注准20252070227 | 2025年10月15日 |
| 12 | 肠内营养泵 | 安徽健之缘医械科技有限公司 | 皖械注准20252140226 | 2025年10月15日 |
| 13 | 手动轮椅车 | 安徽驿康运动科技有限公司 | 皖械注准20252190225 | 2025年10月14日 |
| 14 | 婴儿颅骨矫形固定器 | 蚌埠崇迪生物科技有限公司 | 皖械注准20252040224 | 2025年10月10日 |
| 15 | 一次性使用无菌手术膜 | 安徽富美医疗科技有限公司 | 皖械注准20252140223 | 2025年10月10日 |
| 16 | 医用冷藏箱 | 安徽源君生物科技有限公司 | 皖械注准20252220222 | 2025年10月9日 |
| 17 | 白介素6检测试剂盒(荧光免疫层析法) | 必欧瀚生物技术(合肥)有限公司 | 皖械注准20252400221 | 2025年10月1日 |
| 18 | 无线电子体温计 | 中科瑞峰(安徽)医疗科技有限公司 | 皖械注准20252070220 | 2025年10月1日 |
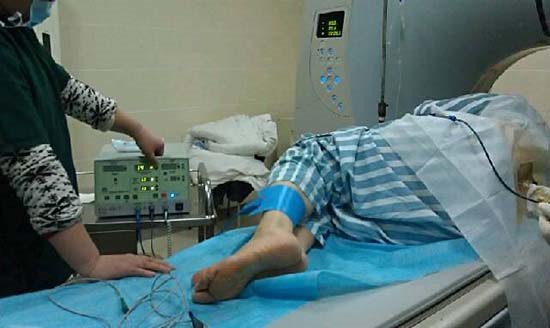
小知识:
运输稳定性验证通常在医疗器械申请过程中被忽视,尤其是对温度敏感(如生物活性试剂)。、对易碎性(如玻璃内窥镜)或无菌设备。按照ASTMM,这种验证需要模拟从出厂到临床使用的全运输链的潜在危害。 D4169、ISTA 3E与其他标准构建了一个测试模型,包括空运、运输与多式联运。验证的主要内容包括:温度与湿度极限挑战(例如-40℃-55℃循环试验下的试剂活性衰减率)≤5%)、机械冲击保护(模拟9米/秒²加速冲击后精密零件的位移量≤0.1mm)保持包装完整性(无菌屏障密封强度在5-500Hz下的振动频率)≥因此,对于需要冷链运输的设备,必须对温度监测设备的精度开展额外的验证。(±0.5℃及断电应对策略(例如,保持相变材料2-8℃的时间长度。≥因此,经典案例表明,一个微创手术机器人需要补充低压舱测试数据,因为它没有模拟高原低气压(等效海拔4000米)的运输环境,结果液压系统气蚀失效。因此,在申请申报时,运输验证报告应弄清楚最差的运输方式(如“上海-乌鲁木齐”陆空联运)、包装产品老化相关性(例如,泡沫聚氨酯缓冲指数衰减50次压缩后)≤10%)与开启包装后的重复使用次数(例如,开关回收测试后5次),这种验证不仅关系到产品临床使用的稳定性,也是供应链潜在危害管理的主要依据。


 1365
1365

