医疗器械真实世界数据 采集要求
1范围
本文件给出了目前常见医疗器械临床评价真实世界数据采集要求,包括常用数据集、变量名称、变量编码。
本文件适用于医疗器械临床评价真实世界数据。
2 规范性引用文件
下列文件中的内容通过文中的规范性引用而构成本文件必不可少的条款。其中,注日期的引用文件,仅该日期对应的版本适用于本文件;不注日期的引用文件,其最新版本(包括所有的修改单)适用于本 文件。
YY/T XX 医疗器械真实世界数据术语与定义
YY/T 1930-2024医疗器械临床评价 术语与定义
YY/T 1956-2025 体外诊断试剂临床试验术语与定义
GB/T 14396-2016疾病分类与代码
T/CHIA 001-2017 手术、操作分类与代码
WS/T 364-2023 卫生健康信息数据元值域代码标准
3 术语与定义
3.1 真实世界数据real-world data;RWD
即传统临床试验以外的,从多种来源收集的各种与患者健康状况与/或常规诊疗及保健密切相关的数 据。
[来源:《真实世界数据用于医疗器械临床评价技术指导原则(试行)》,一(一)]
3.2 真实世界证据real-world evidence;RWE
通过研究真实世界数据,形成医疗器械使用、风险/收益相关的临床证据。
[来源:《真实世界数据用于医疗器械临床评价技术指导原则(试行)》,一(一)]
3.3 真实世界研究real-world study;RWS
围绕相关科学问题,综合运用流行病学、生物统计学、循证医学等多学科方法技术, 利用真实世界 数据开展的研究。
[来源:《真实世界数据用于医疗器械临床评价技术指导原则(试行)》,一(一)]
3.4 原始数据集original dataset
一致主题下多个变量的集合,这些变量的观测值共同形成该原始数据集。
[来源:《医疗器械临床试验数据递交要求注册审查指导原则》,四(一)]
3.5 原始数据库original database
常包括从病例报告表与外部文件中直接收集的原始数据,通常由多个不同的原始数据集组成。
[来源:《医疗器械临床试验数据递交要求注册审查指导原则》,四(一)]
3.6 研究数据库analysis database
为便于统计研究使用原始数据集形成的数据库,用于产生临床试验报告中的统计结果。
[来源:《医疗器械临床试验数据递交要求注册审查指导原则》,四(二)]
3.7 不良事件adverse event;AE
医疗器械在使用过程中出现的不良医学事件,无论是否与医疗器械相关
[来源:YY/T1930-2024 医疗器械临床评价 术语与定义]
3.8 严重不良事件 serious adverseevent;SAE医疗器械临床试验过程中出现的结果死亡或者健康状况严重恶化,包括致命的疾病或者伤害、身体结构或者身体功能的永久性缺陷、需要住院治疗或者延长住院时间、需要采取医疗措施以避免对身体结 构或者身体功能造成永久性缺陷;结果胎儿窘迫、胎儿死亡或者先天性异常、先天缺损等的事件。
[来源:YY/T1930-2024 医疗器械临床评价 术语与定义]
3.9 器械相关不良事件adverse device effect; ADE
医疗器械在使用过程中出现的与器械相关的不良医学事件。
[来源:YY/T1930-2024 医疗器械临床评价 术语与定义]
3.10 器械缺陷 devicedeficiency
医疗器械在正常使用情况下,存在可能危及人体健康与生命安全的不可靠风险,如标签错误、质量问题、故障等。
[来源:YY/T1930-2024 医疗器械临床评价 术语与定义]
3.11 患者自报结局 patient-reported outcome; PRO
是一种来自患者自身测量与评价疾病结局的指标,包括症状、生理、心理、医疗服务满意度等。其 记录有纸质与电子可归结成两种方式,后者称为电子患者自报结局(ePRO)。
[来源:《用于产生真实世界证据的真实世界数据指导原则(试行)》,二(1)8]
3.12 患者自报数据 patient-reported data
患者通过自我检测健康状况提供的健康数据。
[来源:《用于产生真实世界证据的真实世界数据指导原则(试行)》,二(1)8]
3.13 前瞻性研究 prospective study
在研究开始时确定目标人群,并于该时间点以后收集暴露/治疗与结局数据的研究。
[来源:FDA《Use ofReal-World Evidence toSupport Regulatory Decision-Making for Medical device》]
3.14 通过了解性研究 retrospectivestudy
通过历史数据(即研究启动之前生成的数据)定义目标人群并确定暴露/治疗的研究。在研究开始 时,就已经确定相关变量与结局。
[来源:FDA《Use ofReal-World Evidence toSupport Regulatory Decision-Making for Medical device》]
3.15 常规收集的健康医疗数据 routinely collected health data; RCD
基于临床或管理目的收集的健康医疗数据,这些数据的产生无预先设定的研究目的,包括医院电子 病历数据、医疗保险理赔数据等。
[出处:重新认识真实世界数据研究:更新与展望,王雯等,中国循证医学杂志 2020;Langanetal., BMJ2018]
4 数据集与变量
4.1 人口统计学信息
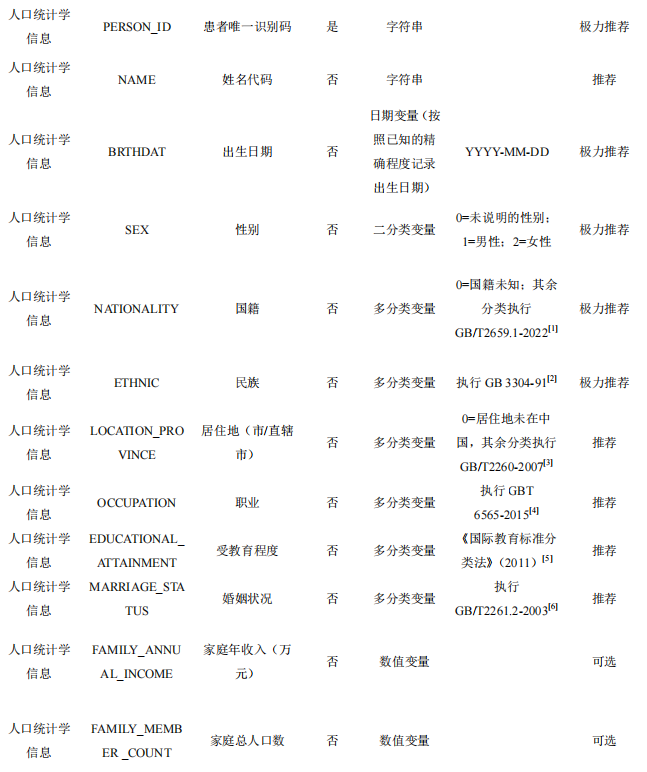
本数据集收集患者的人口学统计信息,包括出生日期、性别、民族、教育水平等信息。
表1 人口统计学信息数据表单


4.2个人史
本数据集收集患者的个人史,主要包括吸烟、饮酒与身体活动等信息。
表2 个人史数据表单
数据集 | 变量名 | 变量 标签 | 索引 变量 | 变量 格式/类型 | 变量编码 | 变量 推荐程度 |
个人史 | REGISTRATIO N_DATE_PERS ONAL_ | 个人史表单登 记日期 | 否 | 日期变量 | YYYY-MM-DD | 极力推荐 |
个人史 | HISTORY PERSON_ID | 患者唯一识别 码 | 是 | 字符串 | 极力推荐 | |
个人史 | SMOKING | 是否吸烟 | 否 | 二分类变量 | 1=是;2=否 | 极力推荐 |
个人史 | SMOKING_DU RATION | 烟龄 | 否 | 数值 | 推荐 | |
个人史 | SMOKING_CO NSUMPTION | 日吸烟量 | 否 | 数值 | 推荐 | |
个人史 | SMOKING_QU IT | 是否戒烟 | 否 | 二分类变量 | 1=是;2=否 | 推荐 |
个人史 | SMOKING_QU IT_DURATION | 戒烟年数 | 否 | 数值 | 推荐 | |
个人史 | DRINKING | 是否饮酒 | 否 | 二分类变量 | 1=是;2=否 | 极力推荐 |
个人史 | DRINKING _ DURATION | 饮酒年数 | 否 | 数值 | 推荐 | |
个人史 | DRINKING | 日饮酒量 | 否 | 数值 | 推荐 |
个人史 | _CONSUMPTI ON DRINKING_Q UIT | 是否戒酒 | 否 | 二分类变量 | 1=是;2=否 | 推荐 |
个人史 | DRINKING_Q UIT_DURATIO N | 戒酒年数 | 否 | 数值 | 推荐 | |
个人史 | BAD_DIETAR Y_PATTERNS | 与疾病紧密相 关的饮食习惯 | 否 | 多分类变量 | 推荐 | |
个人史 | RED_MEAT_D IETARY | 红肉及加工肉 类饮食 | 否 | 二分类变量 | 1=是;2=否 | 可选 |
个人史 | HIGH_SODIU M_INTAKE | 高盐饮食 | 否 | 二分类变量 | 1=是;2=否 | 可选 |
个人史 | PASSIVE_SMO KING | 二手烟 | 否 | 二分类变量 | 1=是;2=否 | 可选 |
个人史 | VACCINATIO N | 与疾病相关的疫苗接种 | 否 | 多分类变量 | 可选 | |
个人史 | OCCUPATION AL _EXPOSURE | 不良影响职业 暴露 | 否 | 多分类变量 | 紫外射线、氡气(室 内放射性气体)、石 棉、砷、柴油废气等 | 可选 |
4.3既往病史
本数据集收集患者的既往疾病史(含手术史),包括既往所患疾病名称、诊断时间与疾病转归等信息。
表3既往病史数据表单
数据集 | 变量名 | 变量 标签 | 索引 变量 | 变量 格式/类型 | 变量编码 | 变量 推荐程度 |
既往病史 | REGISTRATIO N_DATE_MED ICAL_ HISTORY | 既往史表单登 记日期 | 否 | 日期变量 | YYYY-MM-DD | 极力推荐 |
既往病史 | PERSON_ID | 患者唯一识别 码 | 是 | 字符串 | 极力推荐 | |
既往病史 | MHTERM | 疾病名称 | 否 | 多分类变量 | 执行《疾病分类 与代码》 | 极力推荐 |
既往病史 | MHSTDAT | 疾病首次诊断 时间 | 否 | 日期变量 | (GB/T14396-2 016)[7] YYYY-MM-DD | 推荐 |
既往病史 | MHONGO | 疾病转归 | 否 | 多分类变量 | 1=完全康复,2= 不完全康复,3= 死亡 | 推荐 |
手术史 | REGISTRATIO N_DATE_PRO CEDURE_HIS TORY | 手术史表单登 记日期 | 否 | 日期变量 | YYYY-MM-DD | 可选 |
手术史 | PROCEDURE_ _HISTORY_N AME | 手术名称 | 否 | 多分类变量 | 详见附件 《手 术、操作分类与 代码》(T/CHIA 001-2017) | 可选 |
手术史 | PROCEDURE_ | |||||
手术史 | _HISTORY_DA TE | 手术操作日期 | 否 | 日期型 | YYYY-MM-DD | 可选 |
PROCEDURE_ | ||||||
HISTORY_HO | 手术医院 | 否 | 字符串 | 可选 | ||
SPITAL |
4.4家族史
本数据集收集患者直系三代亲属的疾病史,包括患疾病名称、诊断时间与疾病转归等信息。
表4 家族史数据表单
数据集 | 变量名 | 变量 标签 | 索引 变量 | 变量 格式/类型 | 变量编码 | 变量 推荐程度 |
家族史 | REGISTRATIO N_DATE_FAMILY | 家族史表单登 记日期 | 否 | 日期变量 | YYYY-MM-DD | 极力推荐 |
家族史 |
PERSON_ID | 患者唯一识别 码 | 是 | 字符串 | 极力推荐 |
家族史 | FAMILY_RELATIONSHIP | 家庭关系 | 否 | 多分类变量 | 执行《家庭关系 代码》 (GB/T4761-20 08)[8] 执行《疾病分类 | 推荐 |
家族史 | MHTERM | 疾病名称 | 否 | 多分类变量 | 与代码》 (GB/T14396-2 016)[7] | 推荐 |
家族史 | MHSTDAT | 疾病首次诊断 时间 | 否 | 日期变量 | YYYY-MM-DD | 推荐 |
家族史 | MHENDDAT | 疾病结束时间 | 否 | 日期变量 | YYYY-MM-DD | 推荐 |
家族史 | MHONGO | 疾病转归 | 否 | 多分类变量 | 1=完全康复,2= 不完全康复,3= 死亡 | 推荐 |
4.5现病史
本数据集收集患者的现病史,包括既往所患疾病名称、诊断时间、疾病分期与分级等信息。
表5 现病史数据表单
数据集 | 变量名 | 变量 标签 | 索引 变量 | 变量 格式/类型 | 变量编码 | 变量 推荐程度 |
现病史 | REGISTRATIO N_DATE_DISE ASE | 现病史表单登 记日期 | 否 | 日期变量 | YYYY-MM-DD | 极力推荐 |
现病史 | PERSON_ID | 患者唯一识别 码 | 是 | 字符串 | 执行《疾病分类 | 极力推荐 |
现病史 | MHTERM | 疾病名称 | 否 | 多分类变量 | 与代码》 (GB/T14396-2 016)[7] | 极力推荐 |
现病史 | MHSTDAT | 疾病初次诊断 时间 | 否 | 日期型 | YYYY-MM-DD | 极力推荐 |
现病史 | STAGE_OF_DI SEASE | 疾病分期 | 否 | 多分类变量 | 按照疾病属性 开展填写,如 1=0期;2=I期; 3=II 期;4=III 期;5=IV期 按照疾病属性 | 可选 |
现病史 | CLASSIFICATI ON_OF_DISEA SE | 疾病分级 | 否 | 多分类变量 | 开展填写,如1=轻度;2=中度;3=重度;4= 极重度 | 可选 |
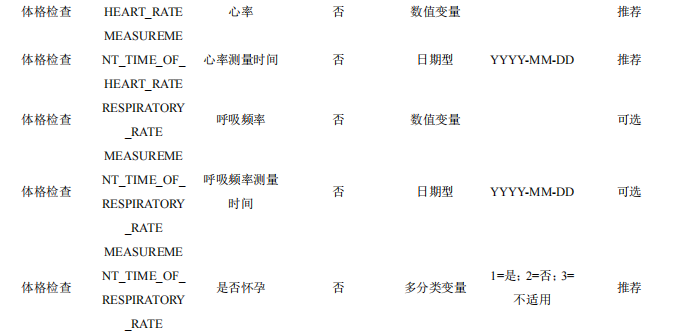
4.6 体格检查
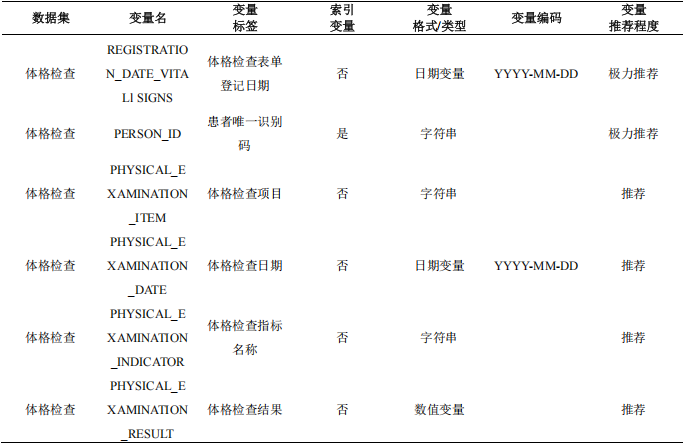
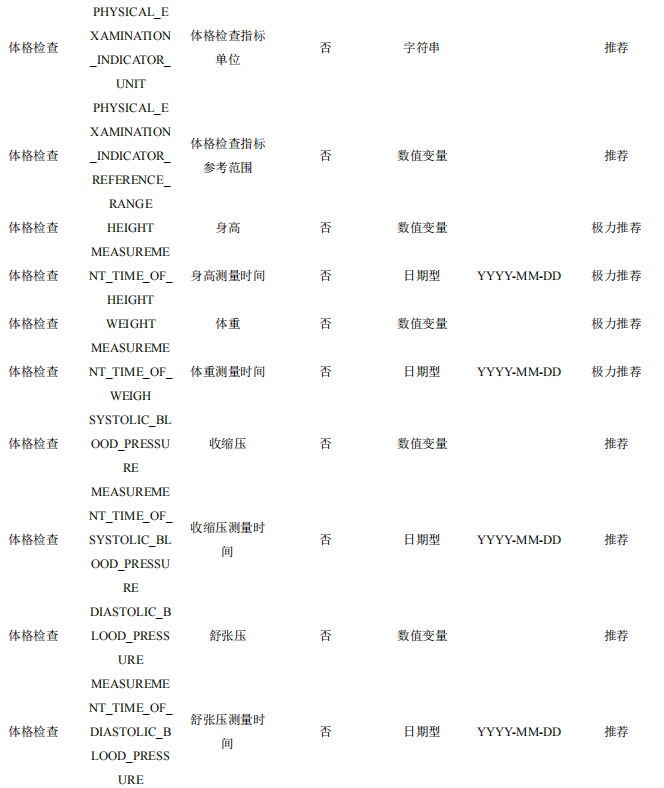
本数据集收集患者的体格检查,主要包括身高、体重、血压与心率等信息,体格检查项目需要按照 研究目的开展。
表6 体格检查数据表单
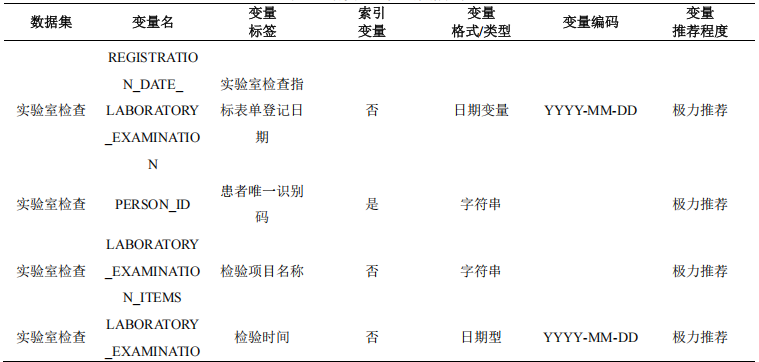
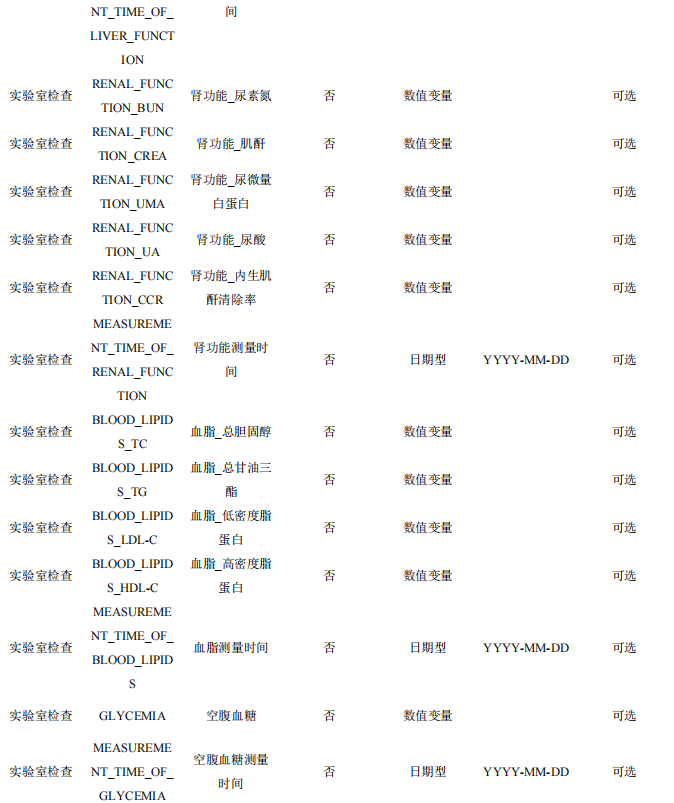
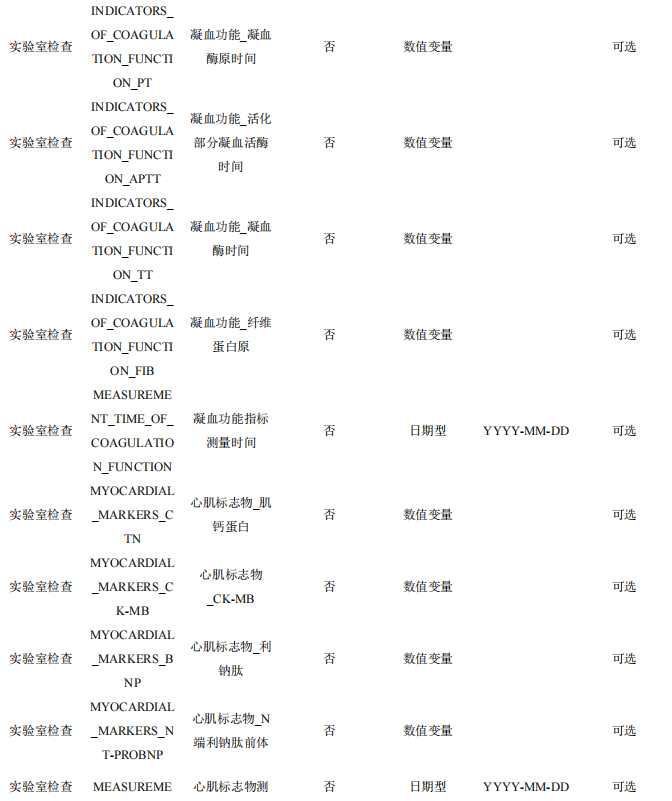
4.7 实验室检查指标
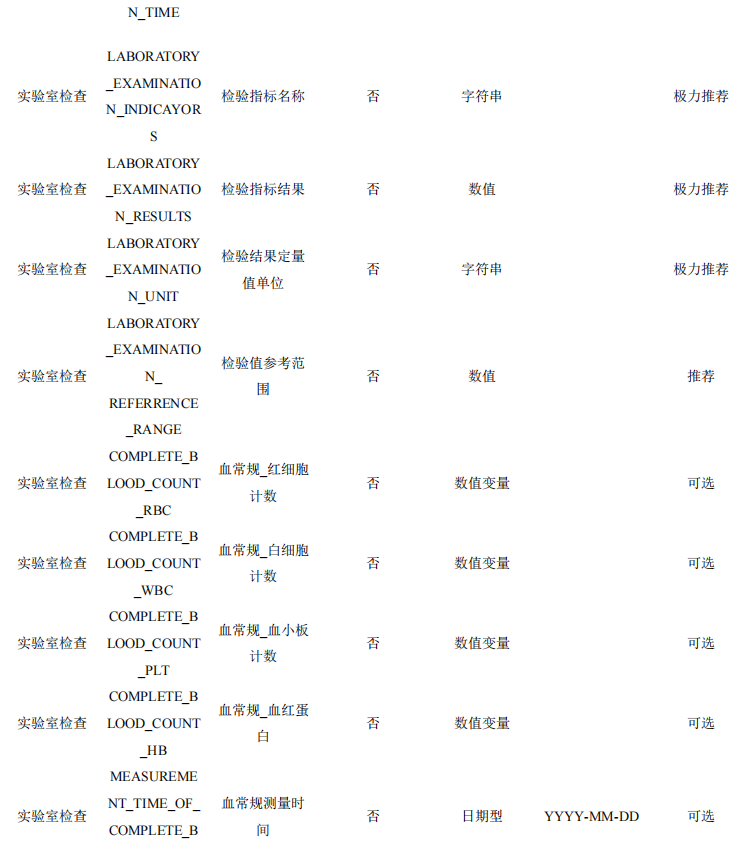
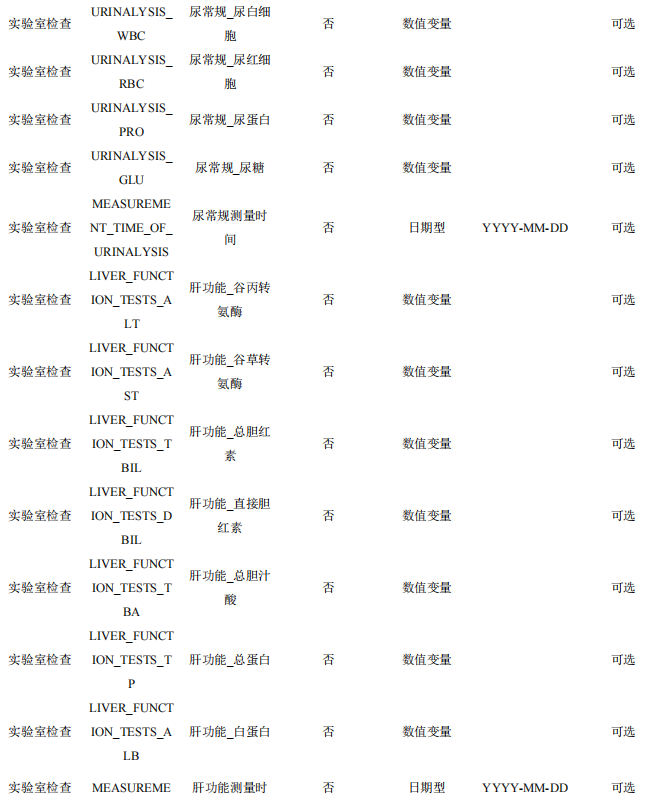
本数据集收集患者的实验室检查指标,主要包括常规检查(如血常规、尿常规等)、生化检查(如肝功能、肾功能、血糖、血脂等) 、免疫学检查(如抗体检测、炎症指标等),按照不同的研究目的可 能会增加其他相关的实验室检查指标。
表7 患者实验室检查数据表单

4.8临床辅助检查
4.8.1 影像学检查指标
本数据集收集患者的影像学检查指标,主要包括影像学检查名称与诊断意见等信息。影像学检查一 般包括,X线检查、超声检查、计算机断层扫描检查、磁共振成像检查、核医学检查等,需要按照研究 所需开展相应的影像学检查。
表8 患者影像学检查数据表单
数据集 | 变量名 | 变量 标签 | 索引 变量 | 变量 格式/类型 | 变量编码 | 变量 推荐程度 |
影像学检查 | REGISTRATIO N_DATE_ IMAGING_EX AMINATION | 影像学检查表单登记日期 | 否 | 日期变量 | YYYY-MM-D D | 极力推荐 |
影像学检查 | PERSON_ID | 患者唯一识别 码 | 是 | 字符串 | 极力推荐 | |
影像学检查 | IMAGING _EXAMINATI ON_ITEMS | 影像学检查名 称 | 否 | 字符串 | 推荐 | |
影像学检查 | IMAGING _EXAMINATI ON_SITE | 影像学检查部 位 | 否 | 字符串 | 推荐 | |
影像学检查 | IMAGING _EXAMINATI ON_ TIME | 影像学检查时 间 | 否 | 日期型 | YYYY-MM-D D | 推荐 |
影像学检查 | DIAGNOSTIC _OPINION | 诊断意见 | 否 | 字符串 | 推荐 |
4.8.2功能检查
本数据集收集患者的功能检查指标,主要包括功能检查名称与诊断意见等信息。功能检查一般包括,心电图、脑电图、肺功能检查等,需要按照研究所需开展相应的功能检查。
表9 患者功能检查数据表单
数据集 | 变量名 | 变量 标签 | 索引 变量 | 变量 格式/类型 | 变量编码 | 变量 推荐程度 |
功能检查 | REGISTRATIO N_DATE_ FUCTION_EX AMINATION | 功能检查表单 登记日期 | 否 | 日期变量 | YYYY-MM-D D | 极力推荐 |
功能检查 | PERSON_ID | 患者唯一识别 码 | 是 | 字符串 | 极力推荐 | |
功能检查 | FUCTION _EXAMINATI ON_ITEMS | 功能检查名称 | 否 | 字符串 | 推荐 | |
功能检查 | FUCTION _EXAMINATI ON_SITE | 功能检查部位 | 否 | 字符串 | 推荐 | |
功能检查 | FUCTION _EXAMINATI ON_ TIME | 功能检查时间 | 否 | 日期型 | YYYY-MM-D D | 推荐 |
功能检查 | DIAGNOSTIC _OPINION | 诊断意见 | 否 | 字符串 | 推荐 |
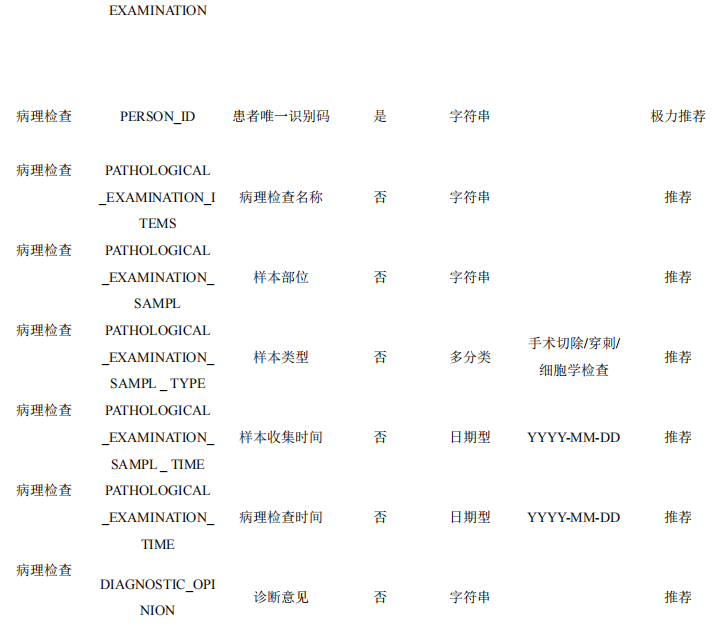
4.9 病理检查
本数据集收集患者的病理检查指标,主要包括病理检查名称与诊断意见等信息。病理检查一般包括,组织活检、细胞学检查、分子检测等,需要按照研究所需开展相应的病理检查。
表10 患者病理检查数据表单

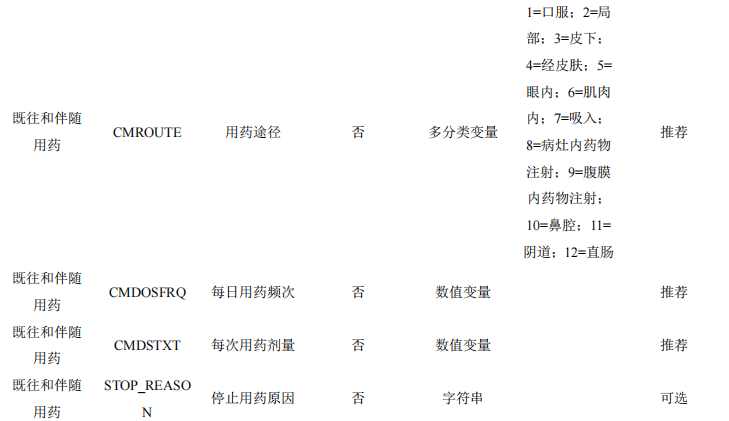
4.10既往与伴随用药
本数据集收集患者的既往用药与伴随用药,包括药品通用名、剂型、用药途径与停止用药原因等信 息。
表11 患者用药数据表单


4.11 诊疗服务
本数据集收集患者的诊疗服务信息,包括门诊就诊、住院记录、急诊就诊等信息。
表12 患者诊疗服务数据表单
数据集 | 变量名 | 变量 标签 | 索引 变量 | 变量 格式/类型 | 变量编码 | 变量 推荐程度 | |
诊疗服务 | REGISTRATIO N_DATE_VISI T | 诊疗服务表单登记日期 | 否 | 日期变量 | YYYY-MM-DD | 极力推荐 | |
诊疗服务 | PERSON_ID | 患者唯一识别码 | 是 | 字符串 | 极力推荐 | ||
诊疗服务 | VISIT_TYPE | 就诊类型 | 否 | 多分类变量 | 1= 门诊;2=急 诊;3=住院;4=非医疗机构就诊 | 推荐 | |
诊疗服务 | HOSPITAL_NAME | 医院名称 | 否 | 字符串 | 推荐 | ||
诊疗服务 | HOSPITAL_LE | 医院等级 | 否 | 多分类变量 | 1=三级;2=二 | 推荐 | |
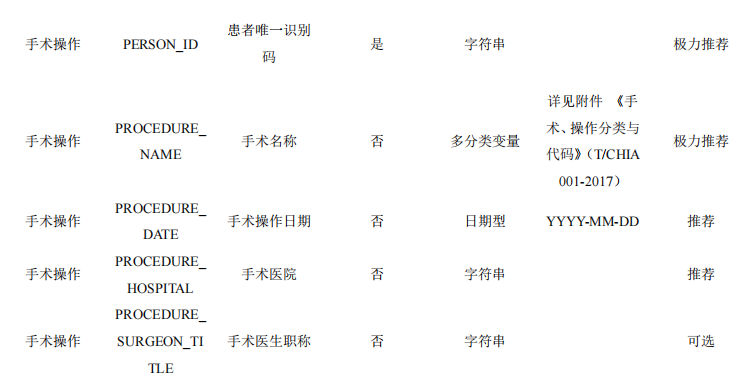
4.12手术操作
本数据集收集患者的手术操作信息,包括手术名称、手术操作日期等信息。因研究目的不同,可能 部分研究不涉及手术操作。
表13 患者手术操作数据表单

4.13医疗器械信息
本数据集收集医疗器械相关信息,包括医疗器械名称、医疗器械唯一标识码、医疗器械的使用方 式、医疗器械开始使用日期、医疗器械结束使用日期与医疗器械停用原因等信息。
表14 医疗器械信息数据表单
数据集 | 变量名 | 变量 标签 | 索引 变量 | 变量 格式/类型 | 变量编码 | 变量 推荐程度 |
医疗器械信息 | REGISTRATIO N_DATE_ PRODUCT | 医疗器械表单登记日期 | 否 | 日期变量 | YYYY-MM-D D | 极力推荐 |
医疗器械信息 | PERSON_ID | 患者唯一识别 码 | 是 | 字符串 | 极力推荐 | |
医疗器械信息 | PRODUCT_N AME | 产品名称 | 否 | 字符串 | 极力推荐 | |
医疗器械信息 | BRAND_NAM E | 商品名称 | 否 | 字符串 | 可选 |
医疗器械信息 | UDI | 医疗器械唯一 标识 | 是 | 字符串 | 极力推荐 | |
医疗器械信息 | DEVICE_MAN UFACTURER | 制造商 | 否 | 字符串 | 推荐 | |
医疗器械信息 | DEVICE_REGI STRANT DEVICE_FILI | 注册人 | 否 | 字符串 | 推荐 | |
医疗器械信息 | NG APPLICANT | 备案人 | 否 | 字符串 | 推荐 | |
医疗器械信息 | DEVICE_MOD EL | 产品型号 | 否 | 字符串 | 推荐 | |
医疗器械信息 | DEVICE_VER SION | 产品规格 | 否 | 字符串 | 推荐 | |
医疗器械信息 | MANUFACTU RING_DATE | 器械生产日期 | 否 | 日期型 | YYYY-MM-D D | 可选 |
医疗器械信息 | PRODUCT_CO DE | 编码 | 否 | 字符串 | 参考《医疗器械 分类规则》[10] | 极力推荐 |
医疗器械信息 | REGISTRATIO N_NUMBER | 注册证编号 | 否 | 字符串 | 可选 | |
医疗器械信息 | DEVICE_DES CRIPTION | 产品描述 | 否 | 字符串 | 推荐 | |
医疗器械信息 | USE_DATE_ST ART | 开始使用日期 | 否 | 日期型 | YYYY-MM-D D | 可选 |
医疗器械信息 | USE_DATE_E ND | 结束使用日期 | 否 | 日期型 | YYYY-MM-D D | 可选 |
医疗器械信息 | DEVICE_DISC ONTINUANCE REASON | 医疗器械停用 原因 | 否 | 字符串 | 推荐 |
4.14 有效性评价指标(治疗类器械)
本数据集收集治疗类医疗器械有效性评价相关指标,包括疾病转归结局指标、疾病转归指标具体值 以及患者自报结局等信息。
表15 治疗类医疗器械有效性评价指标数据表单
数据集 | 变量名 | 变量 标签 | 索引 变量 | 变量 格式/类型 | 变量编码 | 变量 推荐程度 |
有效性评价 指标 | PERSON_ID | 患者唯一识别 码 | 是 | 字符串 | 极力推荐 | |
有效性评价 指标 | EFFECTIVENE S_EVALUATIO | 有效性评价结 局指标 | 否 | 字符串 | 极力推荐 | |
N_INDICATOR | ||||||
有效性评价 指标 | EFFECTIVENE S_EVALUATIO | 数值型结局指 标值 | 否 | 数值变量 | 极力推荐 | |
N_INDEX | ||||||
有效性评价 指标 | EFFECTIVENE S_EVALUATIO | 分类型结局指 标值 | 多分类变量 | 极力推荐 | ||
N_VALUE | ||||||
有效性评价 指标 | EFFECTIVENE S_EVALUATIO | 有效性评价结局测量时间 | 否 | 日期型 | YYYY-MM-DD | 推荐 |
N_DATE | ||||||
有效性评价 指标 | PATIENT_LIV E | 患者是否存活 | 否 | 二分类变量 | 1=是;2=否 | 推荐 |
有效性评价 指标 | PATIENT_LIV E_EVALUATIO | 患者是否存活记录时间 | 否 | 日期型 | YYYY-MM-DD | 推荐 |
N_DATE | ||||||
有效性评价 指标 | PATIENT_REP ORT_INDICAT | 患者自报结局指标名称 | 否 | 字符串 | 推荐 | |
OR | ||||||
PATIENT_REP | ||||||
有效性评价 指标 | ORT_MEASUR EMENT_SCAL E | 患者自报结局 指标测量量表 | 否 | 字符串 | 推荐 | |
有效性评价 指标 | PRO_OUTCO ME | 患者自报结局 指标测量量表 结果 | 否 | 字符串 | 推荐 | |
| 有效性评价 指标 | PRO _MEASUREM ENT _DATE | 患者自报结局指标测量时间 | 否 | 日期型 | YYYY-MM-DD | 推荐 |
4.15 有效性评价指标(体外诊断试剂及诊断器械)
本数据集收集体外诊断试剂及诊断类医疗器械有效性评价相关指标,包括有效性评价结局指标、目 标物检测值、检测结果等信息。
表16 体外诊断试剂及诊断医疗器械有效性评价指标数据表单
数据集 | 变量名 | 变量标签 | 索引变量 | 变量格式/类型 | 变量编码 | 变量推荐程度 |
有效性评价指 | PERSON_ID | 患者唯一识别 | 是 | 字符串 | 极力推荐 | |
标 | 码 | |||||
有效性评价指 | SAMPLE_ID | 样本唯一识别 | 是 | 字符串 | 极力推荐 | |
标 | 码 | |||||
有效性评价指 | LBORRESN1_IN | 目标产品检测 | 否 | 数值变量 | 极力推荐 | |
标 | DEX | 值 | ||||
有效性评价指 | LBORRESN2_IN | 比较方法检测 | 否 | 数值变量 | 极力推荐 | |
标 | DEX | 值 | ||||
有效性评价指 | EFFECTIVENES_ | 目标产品分类 | 多分类变量 | [1|阳性,2|阴 | 极力推荐 | |
标 | EVALUATION_VALUE1 | 型结果指标值 | 性,7|无效,] | |||
有效性评价指 | EFFECTIVENES_ | 比较方法分类 | 多分类变量 | [1|阳性,2|阴 | 极力推荐 | |
标 | EVALUATION_VALUE2 | 型结果指标值 | 性,7|无效,] | |||
有效性评价指 | LBORRESN_CO | 与比较方法检 | 是 | 多分类变量 | [1|一致,2|纷歧 | 极力推荐 |
标 | NSISTENCY_EV ALUATION | 测的一致性指标 | 致,7|无效,] | |||
有效性评价指 | MHDIAG_CONSI | 与临床诊断的 | 是 | 多分类变量 | [1|一致,2|纷歧 | 极力推荐 |
标 | STENCY_EVALUATION | 一致性指标 | 致,7|无效,] | |||
有效性评价指 | LBORRESN3_IN | 内标检测值 | 否 | 数值变量 | 推荐 | |
标 | DEX |
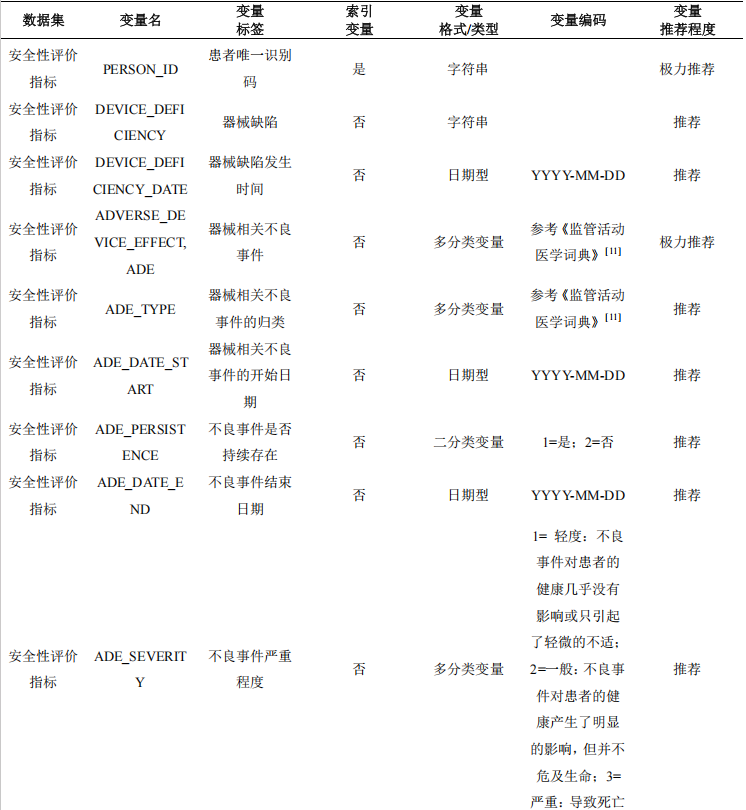
4.16 安全性评价指标
本数据集收集医疗器械安全性相关指标,包括出现器械故障名称、器械不良事件名称等信息。
表17 医疗器械安全性评价指标数据表单

5 数据集的使用
5.1 数据集的使用场景
在以医疗器械临床评价为目的真实世界数据收集与建库过程中,包括基于前瞻性收集数据开展建库 与基于常规收集健康医疗数据(RCD)开展建库2种模式,均可使用本数据标准。
在前瞻性数据收集过程中,可应用本数据标准制作病例报告表(CRF),用以规范、标准化的收集与储存数据。
在基于常规收集健康医疗数据开展建库的过程中,可以使用本标准数据集制定变量提取表单、变量 编码规则,用以规范、标准化的收集与储存数据。
数据采集过程需遵守国家法规。
5.2 变量推荐程度使用的说明
本文件对数据集中的所有字段,开展了变量推荐程度的标记。研究者按照具体的器械品种与研究目 的,原则上需要纳入“极力推荐”的变量,并优先考虑纳入“推荐”的变量,“可选”的变量可作为补 充性字段纳入。
5.3 对标准数据集中变量的扩充
研究者可以按照具体的器械品种与研究目的,按照需求对本文件中未包括的变量开展扩充,收集更 全面的变量信息,用于医疗器械临床评价。
参考文献
[1] GB/T2659.1-2022 世界各国与地区及其行政区划名称代码第1部分国家与地区代码
[2] GB 3304-91中国各民族名称的罗马字母拼写法与代码
[3] GB/T2260-2007中华人民共与国行政区划代码
[4] GBT6565-2015 职业分类与代码
[5] ISCED2011国际教育标准分类法
[6] GB/T2261.2-2003 个人基本信息分类与代码第2部分:婚姻状况代码
[7] GB/T14396-2016 疾病分类与代码
[8] GB/T4761-2008 家庭关系代码
[9] WS/T778-2021 药品采购使用管理分类代码与标识码
[10]医疗器械分类规则 ( 国家食品药品监督管理总局令第15号 ) (https://www.nmpa.gov.cn/ylqx/ylqxfgwj/ylqxbmgzh/20150714120001554.html)
[11]《 监 管 活 动 医 学 词 典 》( MedicalDictionaryforRegulatoryActivities) (https://www.meddra.org/how-to-use/support-documentation/chinese/welcome)


 1408
1408

