被归为分类编码是02 - 12的第二类医疗器械的一次性腹腔镜穿刺器,关于其需要向您开展详细介绍的注册办理流程以及步骤周期,是在符合相关法规要求的基础上,通过一系列包括申请前准备、提交材料、审评审批、获取证书等环节且相互关联、逻辑紧密的程序来完成的,这些环节各自具有特定的操作规范与时间要求,共同构成了整个注册办理的复杂体系。

一、注册准备阶段(1 - 3个月)
(一)弄清楚产品分类与注册单元
确认产品符合第二类医疗器械分类特征,按照产品原理、结构组成、性能指标与适用范围确定注册单元,减少重复检测工作。若产品不在《医疗器械分类目录》内,需向国家药品监督管理局提交《产品分类界定申请》。
(二)启动技术文件准备
在开展产品技术要求的制定工作时需确保其与强制性标准相符,同时开展产品说明书的编写,该说明书需标注“注册证编号预留位置”以及“警示说明”相关内容,且在此过程中还要启动质量管理体系的建设工作,而这一系列任务的推进均需在整体项目规划的框架下有序开展,以保证各项工作之间的协调性与系统性,尽管部分环节的具体实施细节可能仍需进一步细化与弄清楚,但总体的工作方向与任务目标已通过前期的策划与部署得以确定。
二、型式检验阶段(3 - 6个月)
(一)选择检验机构
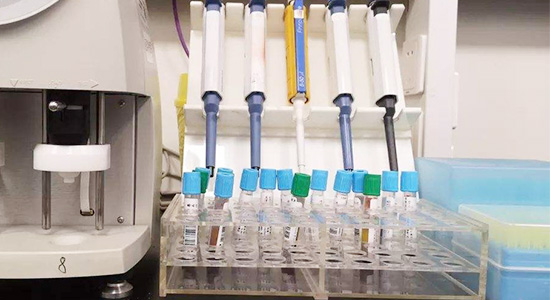
委托国家药品监督管理局认可的医疗器械检验机构开展检验,检验报告需加盖“CMA”“CNAS”资质章。
(二)样品送检与获取报告
送检连续生产的3批合格产品,检验项目覆盖安全性、有效性与可靠性等方面。检测合格后获取《型式检验报告》,若不合格需整改并重测。
三、质量管理体系核查阶段(2 - 4个月)
(一)形成质量管理体系
境内企业需符合《医疗器械生产质量管理规范》,形成涵盖设计开发、采购、生产、检验、售后的全流程体系;进口企业需提供境外生产场地的体系符合性证明或第三方审核报告。
(二)申请现场核查
向省级药监局提交《质量管理体系核查申请表》,接受生产场地布局、设备校准、人员资质等方面的现场核查。审核通过后获取《质量管理体系核查报告》,若不通过需整改并重新申请核查。
四、临床评价阶段(如需要,6 - 12个月)
若产品无法通过同品种比对或缺乏充分临床数据支持,需开展临床试验;若符合免临床条件,可提交同类产品比较研究报告或临床文献资料开展临床评价。
五、注册申报与审评阶段(3 - 12个月)
(一)提交注册资料
通过国家药品监督管理局网上办事大厅提交注册申请资料,包括产品风险研究资料、产品技术要求、产品检验报告、临床评价资料、产品说明书以及标签样稿、质量管理体系文件等。
(二)配合审评工作
省级药监局对注册资料开展技术审评,评估产品的安全性、有效性与质量可控性。审评过程中可能要求企业补充资料或开展现场核查,企业需积极配合。
六、行政审批与注册证发放阶段(20个工作日)
省级药监局按照技术审评结论作出行政审批决定,符合要求的发表《医疗器械注册证》,有效期5年。自作出审批决定之日起10日内,发表、送达密切相关行政许可证件。
七、周期管理
阶段 | 耗时 | 影响因素 |
|---|---|---|
注册准备 | 1 - 3个月 | 产品分类界定、技术文件准备速度 |
型式检验 | 3 - 6个月 | 检验机构工作效率、产品整改情况 |
质量管理体系核查 | 2 - 4个月 | 体系形成改进程度、现场核查结果 |
临床评价(如需要) | 6 - 12个月 | 临床试验进度、数据质量 |
注册申报与审评 | 3 - 12个月 | 资料完整性、审评意见反馈速度 |
行政审批与发证 | 20工作日 | 药监部门工作效率 |
总计(免临床) | 6 - 8个月 | 各环节工作衔接情况 |
总计(需临床) | 10 - 12个月 | 临床试验开展进度 |
要是您想要办理该医疗器械的注册,建议咨询专业的CRO咨询机构,获取更详细的指导与服务。


 1475
1475

