为落实《关于全面深化药品医疗器械监管改革促进医药产业高质量发展的意见》(国办发〔2024〕53号),按照《医疗器械注册与备案管理措施》(国家市场监督管理总局令第47号),按照《国家药监局关于发布优化全生命周期监管支持高端医疗器械创新发展密切相关举措的公告》(2025年第63号)要求,国家药监局组织制订了《优先审批高端医疗器械目录(2025版)》(以下简称《目录》),现予公布,并就密切相关事宜通告如下:
一、国家药监局对《目录》中的医疗器械注册申请按照《医疗器械注册与备案管理措施》第七十三条第(三)项情形实施优先审批。
二、国家药监局医疗器械技术审评中心按程序对《目录》产品注册申请材料开展审核。审核拟定予以优先审批的,公示审核结果无异议后进入优先审批程序;审核拟定不予优先审批的,告知注册申请人原因并按常规程序办理。
三、本《目录》自公布之日起施行。后续国家药监局将按照需要开展调整。
特此通告。
国家药监局
2025年12月24日
附件 优先审批高端医疗器械目录(2025版)
分类编码 | 产品名称 | 产品技术参数或预期用途 |
05-00 | 硼中子俘获治疗系统 | 通过中子与硼药出现俘获反应产生高杀伤力的次级粒子来杀伤癌细胞,用于复发或无其他常规治疗手段的恶性肿瘤的治疗。 |
06-09-03 | 超高场磁共振成像设备 | 磁场强度≥5T。 |
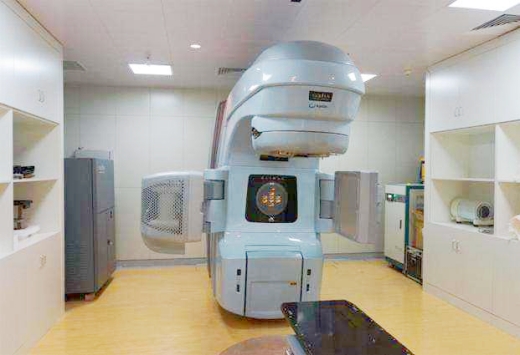
05-01-01 | 医用电子加速器 | 集成了磁共振成像引导的加速器。 |
12-00 19-00 | 植入式脑机接口医疗器械 | 通过植入式电极获取中枢神经系统产生的神经信号,解码与外控设备实时交互或者开展闭环神经调控,用于运动功能障碍、感知功能障碍、言语失能的代偿,或者神经或精神疾病的干预。 |
01-07-03 | 按照基于机器人技术以主从控制方式对手术器械开展操作,经自然腔道对消化道开展手术操作。 | |
13-07-06 | 经导管三尖瓣置换或修复系统 | 适用于重度三尖瓣关闭不全,经临床评估为不适合外科手术的高风险患者。 |
16-07-03 | 微创青光眼手术(MIGS)用植入型青光眼引流装置 | 通过微创青光眼手术,植入眼部形成房水引流通道,用于引流房水。 |
10-06-01 | 膜式氧合器(ECMO用) | 用于需要开展体外膜氧合的患者开展气体交换,能够对呼吸与/或循环衰竭患者开展心肺支持。(仅限于满足以下条件之一:1.国产产品适用人群为新生儿、儿童;2.按照基于国产中空纤维膜组件;3.按照基于国产粒料制备的中空纤维膜组件) |


 1440
1440

