鼻中隔固定器通常上、下夹片连为一体,其内部分呈鸭嘴形,或为扁长状,二端渐尖。无菌提供。用于手术中暂时(小于24h)支撑、固定、复位鼻中隔。鼻中隔固定器在我国属于第一类医疗器械备案产品,分类编码为02-15-03,管理类别为Ⅰ类。
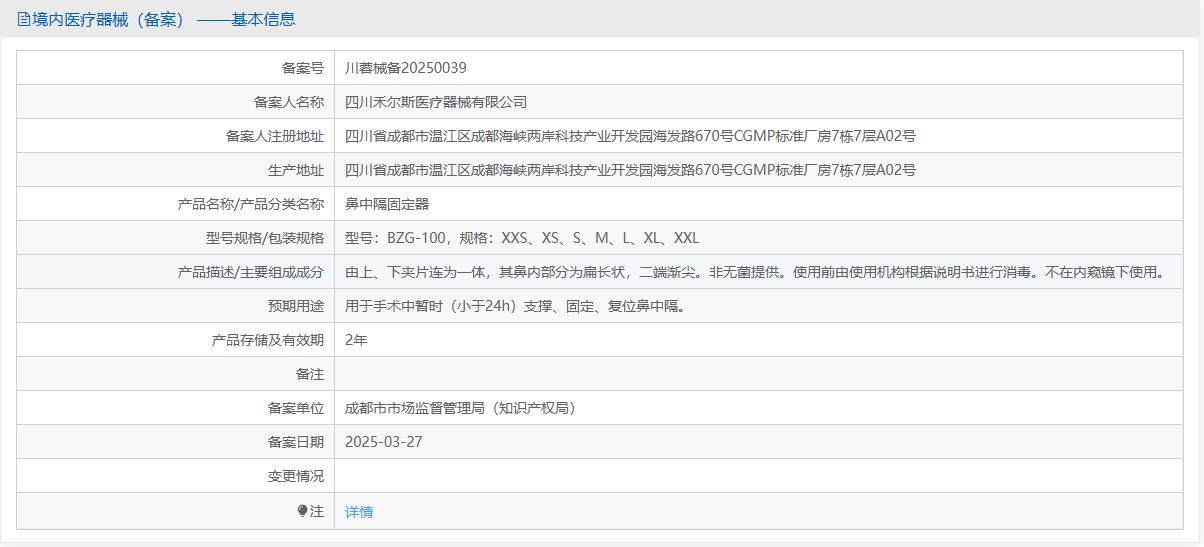
(一)产品分类界定:按照《医疗器械分类目录》,鼻中隔固定器归属"02无源手术器械"子目录,"15手术器械-其他器械"一级产品分组,二级产品分组为"03固位器械",管理类别为Ⅰ类。
(二)备案流程步骤:第一类医疗器械备案需向所在地设区的市级药品监督管理部门提交备案资料,主要步骤包括:产品技术要求编制、产品检验报告、备案申报资料准备、形式审查、备案凭证发放等。
(三)临床评价要求:第一类医疗器械不需要开展临床评价,直接按照备案要求提交相关资料即可。Ⅰ类医疗器械风险程度低,不需要提交临床评价资料。
(四)备案周期:鼻中隔固定器作为第一类医疗器械,备案流程相对简单,整体备案周期通常为15-20个工作日。其中资料准备约需7-10个工作日,形式审查约需5-10个工作日,备案凭证发放即时完成。
如有鼻中隔固定器备案、医疗器械注册及药械相关CRO服务需求,欢迎随时联系飞速度CRO。



 1566
1566

