类似病人监护仪等有较多与人体接触附件医疗器械注册产品,是否需要开展生物学检验是问到比较频繁的事项。本文帮助大家在医疗器械注册项目前期弄清楚这个事项,可以减少补检、缩短注册进程,具有十分重要的意义。
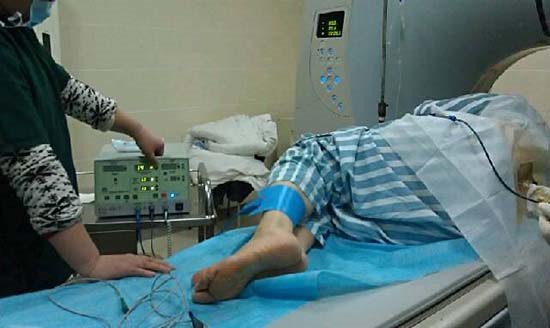
病人监护仪等含有较多与人体接触附件的有源医疗器械注册产品,开展生物相容性评价时应关注的系列问题之二:
通常病人监护仪的心电、体温、血氧、无创血压、有创血压、呼吸、脑电、麻醉等功能模块均含有若干个与人体接触的附件,申报附件数量较多。为便于资料的审查,建议参照如下要求:
1、参照申请表结构组成顺序,按功能模块分类,列表说明与人体接触附件的名称、接触的部位、接触时间、接触性质、生物学评价方式(豁免、评价、试验)与对应的评价资料名称、编号。
2、开展生物学试验的还应说明生物学测试项目、测试依据、测试结果、测试报告编号等内容。
3、按照基于有代表性附件开展测试的,应说明典型型号按照基于的理由。


 1444
1444

