 11-212025
11-212025一次性使用氧气雾化器医疗器械注册技术审评报告(2025年科邦生物版)
一次性使用氧气雾化器用于对液态药物开展雾化,并通过患者吸入,起到预期的治疗效果。产品按照形状不同...... 11-212025
11-212025一次性使用鼻氧管医疗器械注册技术审评报告(2025年三沃医疗版)
一次性使用鼻氧管用于吸氧时氧源与吸氧者之间的氧气直接输送或湿化后输送。产品按结构不同分单鼻塞、头......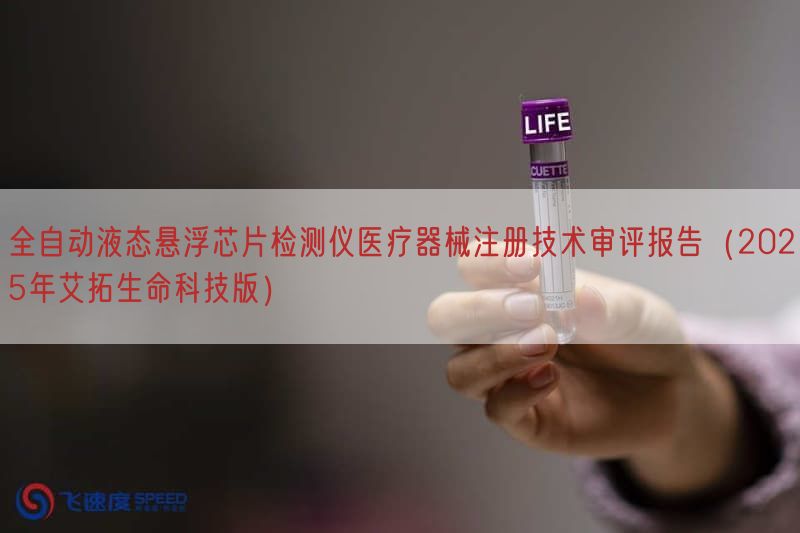 11-212025
11-212025全自动液态悬浮芯片检测仪医疗器械注册技术审评报告(2025年艾拓生命科技版)
全自动液态悬浮芯片检测仪与配套的检测试剂共同使用,用于人体样本中待测物的定性与/或定量检测。产品...... 11-212025
11-212025带附属配件的医疗器械的效期要如何维护?
在医疗机构的医疗设备管理中,保持设备的安全性与有效性是日常工作的至关根本。 对于结构复杂的医疗设...... 11-212025
11-212025近期药监局批准三款创新医疗器械产品,已达381款(附获批创新医疗器械名单)
1、前列腺癌磁共振图像辅助检测软件2025-11-05国家药品监督管理局批准了上海西门子医疗器械...... 11-212025
11-212025福建省25年10月份共批准注册第二类医疗器械产品16个(附名单)
2025年10月,福建省药品监督管理局共批准注册第二类医疗器械产品16个。 特此公告。 ...... 11-212025
11-212025第二类医疗器械注册要点之移动式C形臂X射线机
移动式C形臂X射线机由移动式C形臂机架、X 射线管组件(组合式,2185003)、平板探测器(M...... 11-212025
11-212025第二类医疗器械注册要点之一次性肺结节弹簧圈定位穿刺针
一次性肺结节弹簧圈定位穿刺针由穿刺针、推送杆、弹簧圈及拉线组成。穿刺针由堵帽、护套管、针柄、针管......
请进
提交留言
提交留言



